株式会社三井物産戦略研究所
「個別化」に向かうがん治療
2015年7月6日
三井物産戦略研究所
技術第三室
加藤貴子
Main Contents
がんは遺伝子に異常を起こした細胞が、無秩序に増え続ける病気であることが分かっており、現在その治療は、外科手術、抗がん剤などの薬物療法、放射線治療の3つが基本とされている。そのうち薬物療法においては、効率よくがん細胞を攻撃する薬が開発されたことと、遺伝子解析を行う高度な検査技術の発展により従来の診療情報にがん特有の遺伝情報を合わせることが可能となったことで、最適な治療法が提供される段階に入ってきている。こうした遺伝子レベルでの個人差を見極め、それに合った治療法を選択することは、「個別化医療(Personalized Medicine/Individualized Medicine)」と呼ばれるが、本稿では、個別化医療が進むがん薬物療法の現況を紹介する。
遺伝情報を活用した「がんの個別化医療」とは
がんの医療現場では、遺伝情報を活用することで、より治療効果が高く、かつ副作用の少ない薬物療法の普及が進んでいる。肺がんの薬物療法を例にとってみると、従来は、手術で取り出されたがん病変部を顕微鏡で観察してがんの進行度や悪性度の診断を行い、抗がん剤を投与するのが標準とされてきた。現在ある抗がん剤の多くは、がん細胞だけでなく、口や胃の表面にある細胞や髪の根元にある細胞などさまざまな正常細胞を同じように攻撃してしまうため、重い副作用が伴う。近年、がん発生のメカニズムを遺伝子・分子レベルで解明する研究が進んだことで、がん細胞を狙い撃ちする「分子標的薬」と呼ばれる薬が開発された。肺がんの約8割を占める非小細胞肺がん向けに開発された分子標的薬には、イレッサ、タルセバ、ジオトリフ、ザーコリ、アレセンサがあるが、イレッサ、タルセバ、ジオトリフはEGFR遺伝子1という特定の遺伝子に異常のある患者(肺がん患者の約40%2)に、ザーコリ、アレセンサはALK融合遺伝子1という遺伝子に異常のある患者(同約4%2)に効果的であることが分かっている。従い、患者は自分のがん細胞の遺伝子異常がどこにあるのかを調べる検査を受けることでタイプに合った治療薬を選択することができる。このように遺伝子検査の結果と分子標的薬をマッチングさせることを「がんの個別化医療」と呼んでいる。現在、肺がんにおいては、EGFR遺伝子、ALK融合遺伝子以外にも原因となる遺伝子が数多く見つかっており、個別化が適用されるケースはますます増えるものと考えられる。
「個別化」を可能にした先進技術
がんの個別化医療は、分子標的薬を開発する創薬技術と次世代型の遺伝子解析技術とともに発展している。分子標的薬とは、上述のとおり、がん細胞の異常な遺伝子が作り出す物質を狙って抑えることで、がん細胞の増殖や転移を抑制する薬剤である。現在、世界で60以上3の分子標的薬が承認されており、10年後にはがん薬物療法の中心になるだろうといわれている。
次世代型遺伝子解析は、「次世代シークエンサー(Next Generation Sequencer:NGS)」と呼ばれる画期的な機器が登場したことで、ヒトの全遺伝情報を簡便に検出することが可能となった。もとより遺伝子検査にはいくつかの手法があり、これまでは分子標的薬に関連する複数の遺伝子を1つずつ手間と時間を掛けて検査してきたのだが、NGSを用いることで従来に比べて格段に早く、一度の検査でまとめて結果を得られるようになった。
研究基盤の整備
がんの個別化医療は急速に立ち上がりつつあるが、今後さらに普及させ効果を上げるにはさまざまな取り組みが必要となる。分子標的薬の開発や遺伝子解析研究を牽引してきた米国では、米国国立ヒトゲノム研究所が主導する、遺伝情報と診療情報の統合ネットワーク「The electronic Medical Records and Genomics(eMERGE)Network」の構築や、米国国立がん研究所や製薬会社が共同して分子標的薬の効率的な開発を目指すプロジェクト「Lung-Map trial」等が進められている。また、2015年1月に行われたオバマ大統領の一般教書演説にて、医療現場で遺伝情報や診療情報を積極的に活用する「The Precision Medicine Initiative」の推進を打ち出しており、今後、米国では個別化医療が一層推進されるものと考えられる。
欧州にて個別化医療を先導している英国は、2014年8月、2017年までに10万人のがんおよび希少疾患患者の全遺伝情報を解析し、創薬・治療に活用するプロジェクト「Genomics England」の開始を発表した(予算3億ポンド)。本プロジェクトでは、患者からサンプルを集めて次世代シークエンサーで解析し、得られた全データをデータセンターに集約する。データセンターで、この遺伝情報と診療情報が統合、匿名化され、研究機関および産業界により新たな研究開発のため活用される予定である。
日本は、遺伝子解析研究では欧米と肩を並べる一方、遺伝情報を活用するためのプラットフォーム作りが遅れているが、2015年3月、国立がん研究センター、全国の医療機関(約200施設)、製薬会社(10社)が連携するプロジェクト「SCRUM-Japan」が始動した。本プロジェクトは、2年間で4,500名のがん患者の遺伝子異常をスクリーニングした上で、特定の遺伝子異常を持つ患者に対して個別化医療を提供することを目指している。患者の遺伝情報と診療情報は匿名化後にデータベース化され、新たながん診断・治療薬の研究開発のために活用される予定である。
今後、世界各国でこうした取り組みが進められると予想されるが、遺伝子解析手法の標準化、遺伝子解析結果の質の確保、倫理問題、遺伝情報のセキュリティなど、既に課題として提起されている問題の解決へ向けた動きも同時に加速することが期待される。
医療現場における現状
医療現場では、遺伝子解析を行うことで、医師による分子標的薬選択の意思決定を支援する新たなサービスが始まっている。米国のファンデーション・メディスン社はその先駆的な企業で、自社内のラボに次世代シークエンサーを設置し、医師から送られてきた患者のがん病変部サンプルの遺伝子解析を行い、解析結果を基に推奨される分子標的薬の情報を提供している。現在、提供するサービスは、肺がん、大腸がんなどの固形がん向けの「Foundation One(定価5,800ドル)」、白血病などの血液がん向けの「Foundation One Heme(定価7,200ドル)」の2種類で、検査結果は約2週間で医師にフィードバックされる。2015年1月には、がん領域の医薬品で売上高世界一のロシュ社により買収されており(56%出資で10億ドル)、がんの薬剤療法において遺伝子検査の比重が増していることを示している。また、米国で先進的な医療を提供することで著名なメイヨークリニックが、「Mayo Clinic Center for Individualized Medicine」を設立し、末期がん患者を対象に遺伝子検査を行っている。そのほか、同国で民間病院最大手のホスピタル・コーポレーション・オブ・アメリカ社(がんセンターを75施設保有し、年間約10万件のがん治療を行っている)は、2015年1月、医療ソフトウエアベンチャーの米サイアプス社と提携し診療情報・遺伝情報等のデータを統合し、がん治療の際に医師の診断を支援するシステム「Precision Oncology Platform」を2015年度中に運用開始すると発表するなど、数多くの取り組みが始まっている。
日本でも、前述のファンデーション・メディスン社と同様のサービスが始まっている。2015年3月、IT技術をバイオサイエンス研究に応用するバイオインフォマティクス分野でパイオニア企業である三井情報は、京都大学医学部附属病院から受託する形で、遺伝子検査の結果を医師に提供するサービス「OncoPrime(約88万円)」を国内で初めて開始した。現在、米国に患者サンプルを送付して遺伝子解析を行い、およそ1カ月で医師に検査結果を提供している。
今後の方向性
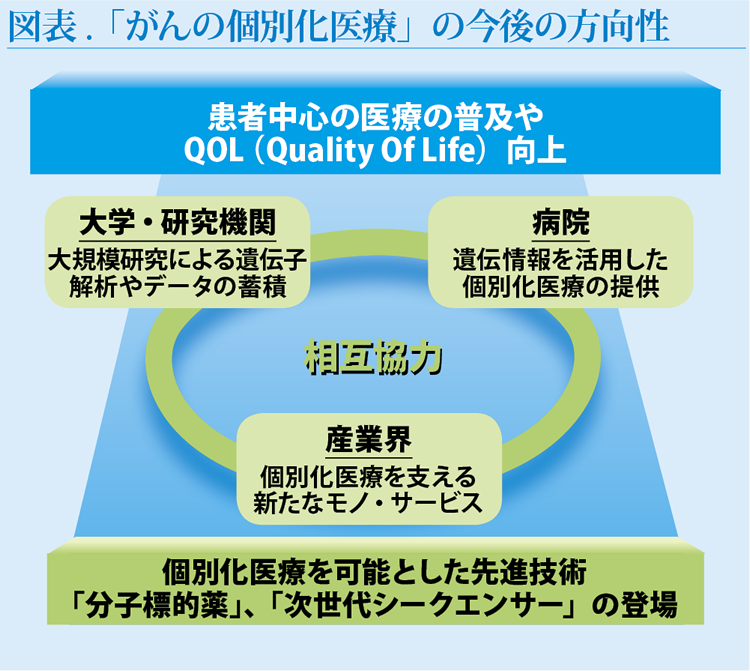
これまでの薬物療法の多くは、平均的な患者向けにデザインされ一様に投与されてきたが、今後はがんの個別化医療が進み、患者中心の医療の普及やQOL(Quality Of Life)向上に寄与するものと考えられる。がんの個別化医療のさらなる推進には、病院、大学・研究機関、製薬会社、遺伝子検査会社、遺伝子解析機器会社、医療情報解析会社などの相互協力が必要で、研究開発、医療現場での提供、その結果のフィードバックがスムーズに行われる仕組みが重要となる(図表)。
本稿では、がん病変部の遺伝子検査に関して取り上げたが、がんの検査技術においては、微量タンパク質、セルフリーDNA4など、ほかにもさまざまな検査技術の開発が進展している。的確な治療は精密な診断の上に成り立つ。医療現場における網羅的な遺伝子解析は始まったばかりだが、今後得られる膨大なデータをいかに患者の治療に役立てるかが求められる。
- 多くのがんでは、無秩序に細胞を増えさせるシグナルが異常に出ている。EGFR遺伝子(Epidermal Growth Factor Receptor遺伝子)とALK融合遺伝子(Anaplastic Lymphoma Kinase遺伝子)は、このシグナル異常に関係する遺伝子。
- 出所:(株)ロハスメディア「がん研が作ったがんが分かる本2015年版」、2015年2月
- 出所:文部科学省新学術領域研究『がん研究分野の特性等を踏まえた支援活動』「化学療法基盤支援活動」ホームページ(2015年2月13日時点)
- セルフリーDNA(Circulating cell-free DNA)とは、血液中を循環しているDNAのこと。がん細胞由来や胎児由来のDNAが血液中で見つかっている。